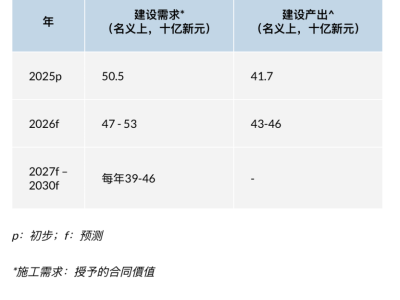
格隆匯3月20日丨復星醫(yī)藥(02196.HK)公告,近日,上海復星醫(yī)藥(集團)股份有限公司控股子公司上海復宏漢霖生物技術股份有限公司及其控股子公司(以下合稱“復宏漢霖”)收到國家藥品監(jiān)督管理局關于同意HLX18(即重組抗PD-1人源化單克隆抗體注射液)用于多種實體瘤治療開展Ⅰ期臨床試驗的批準。復宏漢霖擬于條件具備后于中國境內1開展該藥品的相關臨床研究。
HLX18系集團(即公司及控股子公司/單位,下同)自主研發(fā)的納武利尤單抗生物類似藥,擬用于黑色素瘤、非小細胞肺癌、惡性胸膜間皮瘤、腎細胞癌、經典型霍奇金淋巴瘤、頭頸部鱗狀細胞癌、尿路上皮癌、胃癌、胃食管連接部癌或食管腺癌、食管癌、結直腸癌、肝細胞癌等原研藥已獲批的適應癥。2025年12月,HLX18用于多種實體瘤治療的Ⅰ期臨床試驗申請獲美國FDA(即美國食品藥品監(jiān)督管理局)批準。
截至2026年2月,集團現(xiàn)階段針對HLX18的累計研發(fā)投入約為人民幣0.59億元(未經審計)。根據(jù)IQVIAMIDAS?最新數(shù)據(jù),2025年,納武利尤單抗于全球范圍的銷售額約為117.85億美元。